Electron là gì? Đặc điểm của electron là? Cấu tạo Electron
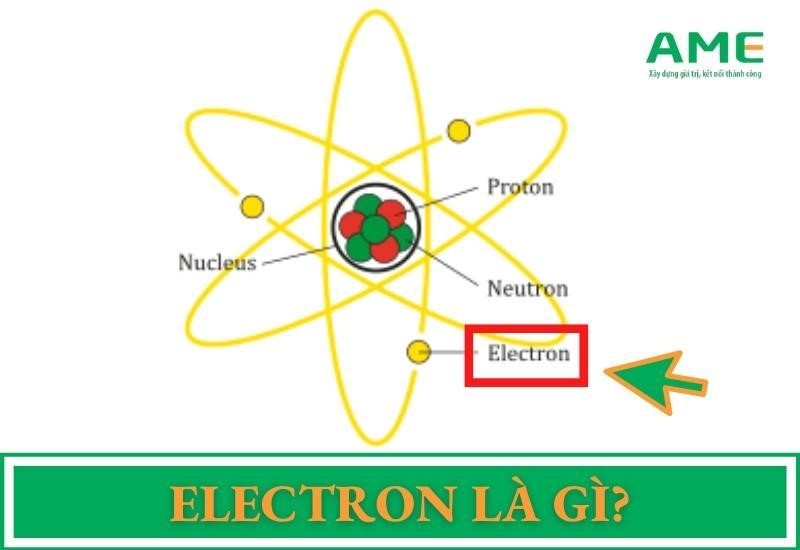
Electron là gì?
Electron là hạt hạ nguyên tử hay điện tử, được ký hiệu là e với điện tích bằng trừ điện tích cơ bản -1,6 x 10-19 Coulomb, khối lượng xấp xỉ bằng 1/1836 lần so với proton (hạt mang điện tích dương). Đây là các hạt mang điện tích âm bao quanh hạt nhân, có vai trò cơ bản nhở nhiều hiện tượng vật lý nwh điện, từ học, hóa học, độ dẫn điện.
Đặc điểm của electron là gì?
Đặc điểm của electron là lực hút do hạt nhân mang điện tích dương tác dụng lên hạt electron mang điện tích âm có nguyên tắc như lực hướng tâm và đóng vai trò cần thiết cho sự quay quanh hạt nhân của các electron. Các electron ở gần hạt nhân sẽ liên kết chặt chẽ với hạt nhân và khó kéo chúng ta khỏi nguyên tử so với các electron ở phía xa
Cấu hình electron
Cấu hình electron là nội dung quan trọng bạn cần nắm được khi tìm hiểu electron là gì. AME Group xin cung cấp cho bạn nội dung chi tiết dưới đây!
Cấu hình electron nguyên tử
Cấu hình electron cho biết sự phân bố electron trên các phân lớp thuộc các lớp khác nhau. Người ta quy ước cụ thể như sau:
- Số thứ tự lớp e là các chữ số 1, 2, 3,…
- Phân lớp được ký hiệu chữ cái thường s, p, d, f,…
- Số e trong 1 phâm lớp là chỉ số mũ của phân lớp s2, p6, d10,…
Lưu ý: Lớp electron ngoài cùng của nguyên tử thể hiện tính chất của 1 nguyên tố:
- Số 2 lớp ngoài cùng tối đa là 8. các nguyên tố này rất bền vững, hầu như không tham gia vào các phản ứng hóa học
- Có 1, 2,3e lớp ngoài cùng thường là nguyên tử kim laoij (trừ H, He, B)
- Có 5,6,7e lớp ngoài cùng thường là phi kim
- Có 4e lớp ngoài cùng có thể là kim loại hoặc phi kim

Mức năng lượng của electron theo các phân lớp
Các bước viết cấu hình electron
Để thực hiện việc viết cấu hình của electron đơn giản, nhanh chóng, bạn thực hiện theo các bước như sau:
- Bước 1: Xác định số electron của nguyên tử dựa vào bảng tuần hoàn hóa học
- Bước 2: Các e được phân bố tăng dần theo thứ tự mức năng lượng AO tuân theo nguyên lý Pau-li và quy tắc Hun
- Bước 3: Viết cấu hình electron thứ tự các phân lớp trong 1 lớp và theo thứ tự của các lớp electron và viết gọn lại.
Ví dụ: Nguyên tử Zn có Z=30
- Ta có số eletron: 30e
- Các lớp e được phân bổ: 1s2 2s2 2p6 3s2 3p6 4s2 3d10
- Do có sự chèn năng lượng của phân lớp 3d với 4s nên ta viết lại như sau: 1s2 2s2 2p6 3s2 3p6 3d10 4s2
- Viết gọn lại [Ar] 3d10 4s2 với [Ar] là cấu hình e của nguyên tố khí hiểm Argon
Cấu tạo của electron
Nhiều người thắc mắc về cấu tạo của hạt e, tuy nhiên electron nhưng không có cấu trúc bên trong và chính nó là 1 hạt điểm với điện tích điểm và không có sự mở rộng ra không gian.
Cấu tạo các hạt cấu thành lên nguyên tử
Nguyên tử là cấu trúc rất nhỏ trong vật chất mà mắt thường không thể nhìn thấy được, kích thước khoảng 10-10 m= 0,1nm.. Cấu tạo của nguyên tử bao gồm hạt nhân và lớp vỏ electron:
- Hạt nhân: Làm ở giữa, bao gồm proton, neutron; có kích thước khoảng 10-14m = 10-5
- Lớp vỏ: Các hạt electron xoay xung quanh không gian hạt nhân
Nguyên tử được cấu tạo từ 3 loại hạt:
- Hạt mang điện tích âm (electron): ký hiệu E, khối lượng 9,1094.10-31kg; điện tích -1,602.10-19C
- Hạt mang điện tích dương (proton): ký hiệu P, khối lượng 1,6726.10-27kg; điện tích +1,602.10-19C
- Hạt mang trung hòa (neutron): ký hiệu N, khối lượng 1,6748.10-27kg; điện tích 0
⇒ Nguyên tử trung hòa về điện khi số hạt proton bằng số hạt electron

Cấu tạo các hạt cấu thành lên nguyên tử
Trên đây là giải đáp chi tiết của AME Group về câu hỏi electron là gì, hy vọng với các thông tin chi tiết trên đây sẽ hữu ích cho bạn. Tiếp tục ủng hộ và theo dõi chúng tôi trong các bài viết tiếp theo nhé!
 Tiếng Việt
Tiếng Việt