Nguyên tử là gì? Mô hình nguyên tử và cấu tạo [Chi tiết]

Một vài thông tin về nguyên tử
Nguyên tử là khái niệm được đề cập từ cách đây rất lâu từ thế kỷ 18, 19. Mỗi loại nguyên tử khác nhau sẽ tương ứng với các nguyên tố khác nhau.
Nguyên tử là gì?
Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi một hay nhiều electron mang điện tích âm. Các nguyên tử có kích thước đường kính rất nhỏ chỉ từ vài phần mười nano mét, khối lượng và thể tích rất nhỏ.
Số hiệu nguyên tử là gì?
Số hiệu nguyên tử là số hạt mang điện hay số proton của nguyên tố hóa học đó, nó cũng chính là số proton tìm thấy trong hạt nhân của 1 nguyên tử. Mỗi nguyên tố hóa học sẽ được xác định duy nhất bởi số hiệu nguyên tử riêng.
Ví dụ Nhôm sẽ có số hiệu nguyên tử là 13, Canxi 20, Kali 19,….
Kí hiệu nguyên tử
Ký hiệu nguyên tử biểu thị đầy đủ các đặc trưng có một nguyên tử của một nguyên tố hóa học. Ký hiệu này cho biết số khối và số hiệu nguyên tử có công thức tổng quát là: ![]()
Trong đó:
- X: Ký hiệu hóa học của của nguyên tố
- A: Số khối
- Z: Số hiệu nguyên tử
Mô hình cấu tạo nguyên tử
Trong mỗi nguyên tử sẽ có cấu tạo cơ bản như sau:
- Lớp vỏ: Những electron mang điện tích âm chuyển động liên tục xoay quanh lớp nhân.
- Hạt nhân: Chứa các hạt mang điện tích dương proton và hạt không mang điện tích neutron
⇒ Nguyên tử được cấu thành từ 3 loại hạt chính gồm electron, proton và notron có điện tích và khối lượng như sau:
- Electron: Điện tích qe = – 1,602 x 10-19 C ; khối lượng me = 9,1094 x 10-31 kg
- Proton: Điện tích qp = –1,602 x 10–19 C; khối lượng mp = 1,6726.10-27kg
- Neutron: Điện tích qn = 0; khối lượng mn = 1,6726.10-27kg
Mô hình sơ đồ cấu tạo nguyên tử chi tiết có lớp vỏ và lớp hạt nhân liên kết bằng các hạt mang điện và không mang điện, có các hạt nhân e và hạt nhường e để tạo ra nguyên tử vững chắc. Quan sát hình ảnh dưới đây:
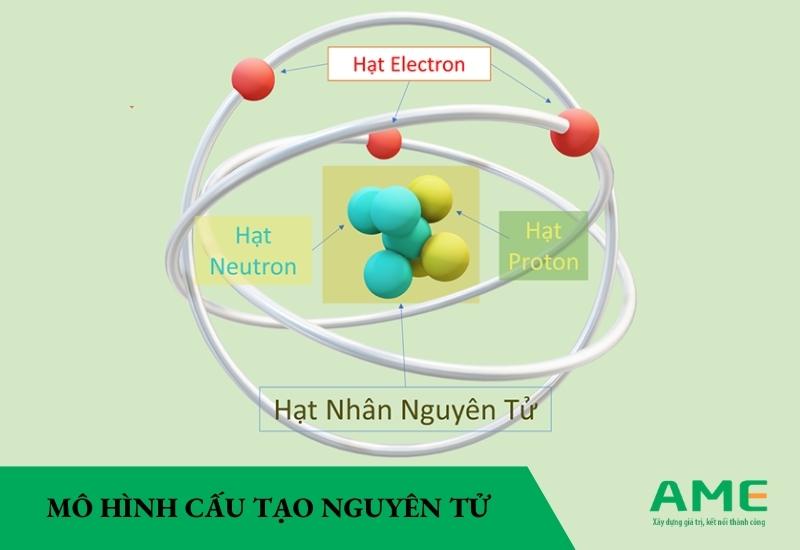
Mô hình cấu tạo nguyên tử
Kích thước và khối lượng của cấu tạo nguyên tử
- Về kích thước, nguyên tử có kích thước rất nhỏ chỉ bằng 10-10 m và hạt nhân khoảng 10-14 Kích thước đơn vị được tính theo đại lượng angstrom (1Å = 10-10m) hoặc nanomet (1nm = 10-9m).
- Về khối lượng, Khối lượng nguyên tử tập trung ở hạt nhân nên khối lượng nguyên tử còn được coi là khối lượng hạt nhân, đơn vị là u (đvC)
1u (đvC) = 1/12 khối lượng 1 nguyên tử C (19,9265.10-27kg) = 1,6605.10-27kg
Khái niệm khác về mô hình nguyên tử
Bên cạnh khái niệm thuần túy về nguyên tử, số hiệu và ký hiệu nguyên tử, bạn cũng cần nắm vững được 1 số khái niệm khác liên quan đến mô hình cầu tạo nguyên tử như sau:
Hạt nhân nguyên tử
Hạt nhân nguyên tử bao gồm các hạt mang điện tích dương (proton) và hạt không mang điện (neutron), mỗi nguyên tử có số p = số e. Trong đó trên 99.94% khối lượng nguyên tử tập trung ở hạt nhân, khối lượng proton và neutron xấp xỉ bằng nhau, khối lượng electron chiếm 1 phần rất nhỏ. Vì vậy người ta coi khối lượng hạt nhân là khối lượng nguyên tử.
Năng lượng nguyên tử là gì?
Năng lượng nguyên tử chính là năng lượng được giải phóng khi xảy ra biến đổi hạt nhân bao gồm năng lượng phân hạch, năng lượng nhiệt hạch, năng lượng do phân rã chất phóng xạ. Đây là năng lượng sóng điện từ có khả năng ion hóa vật chất và năng lượng các hạt được gia tốc.
Mô hình nguyên tử
Mô hình nguyên tử lớp electron (e) gồm có 4 phân lớp bao gồm s, p, d, f với các chức năng khác nhau, càng gần hạt nhân chúng càng nhận được mức năng lượng lớn.
| Phân lớp | s | p | d | f |
| Số e tối đa | 2 | 6 | 10 | 14 |
| Ký hiệu | s2 | p6 | d10 | f14 |
Ví dụ:
- Mô hình nguyên tử nhôm có Z = 13 là 1s22s22p63s23p1
- Mô hình nguyên tử sắt có Z = 26 là 1s22s22p63s23p64s23d6
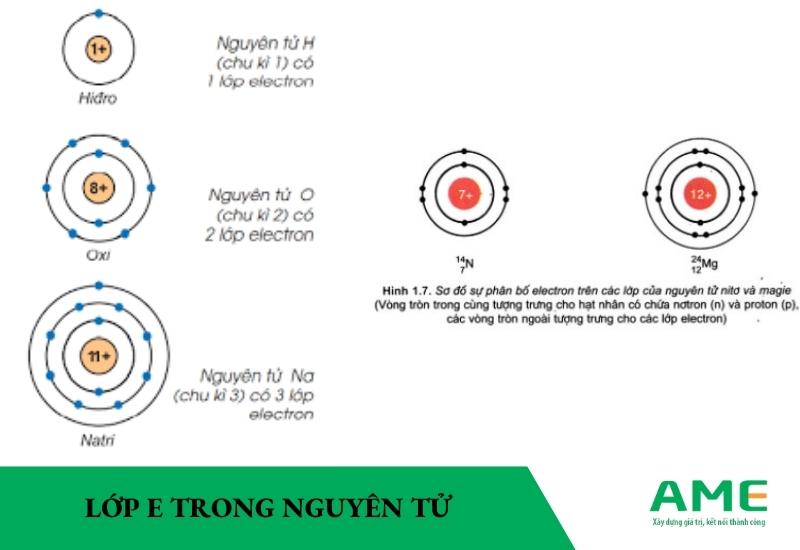
Lớp e trong nguyên tử
Số nguyên tử
Số lượng nguyên tử là số lượng proton có trong hạt nhân nguyên tử của nguyên tố hóa học đó. Nếu nguyên tử không có diện tích thì số lượng nguyên tử bằng số electron.
Nguyên tử khối
Nguyên tử khối là khối lượng một nguyên tử khi tính theo đơn vị Cacbon, môi nguyên tố sẽ có số nguyên tử khối riêng theo đơn vị u (đvC)
1u (đvC) = 1/12 khối lượng 1 nguyên tử Cacbon
Phân biệt nguyên tử và phân tử
Nguyên tử và phân tử là hai khái niệm na ná nhau khiến rất nhiều người nhầm lẫn. AME Group sẽ phân biệt chi tiết cho bạn 2 đại lượng này thông qua bảng dưới đây nhé!
| Tiêu chí | Nguyên tử | Phân tử |
| Khái niệm | Là đơn vị có bản của vật chất gồm các hạt vô cùng nhỏ trung hòa về điện có hạt nhân và bao quanh là các điện tích âm | Bao gồm một số nguyên tử liên kết với nhau, thể hiện tính chất hóa học đầy đủ của 1 chất |
| Ví dụ | Nguyên tử canxi, nguyên tử cacbon, liti,… | Phân tử oxi (O2) ; Phân tử nước (H2O) |
| Hình dáng | Hình cầu | Đa hình dạng |
| Tính chất | Không có khả năng phân đôi | Có thể tách rời các nguyên tố và kết hợp lại với nhau |
| Tồn tại | Có thể tồn tại hoặc không tồn tại trong trạng thái tự do | Tồn tại trong trạng thái tự do |
| Ngoại quan | Không nhìn thấy bằng mắt thường | Không nhìn thấy bằng mắt thường nhưng có thể được khi dùng kính hiển vi |
| Liên kết | Hạt nhân | Cộng hóa trị, cộng ion |
Trên đây là tất tần tật kiến thức và những khái niệm cơ bản nhất về nguyên tử là gì mà bạn cần nắm được. Mỗi nguyên tử sẽ đặc trưng cho 1 nguyên tố khác nhau với số khối, cấu hình electron và các tính chất tương ứng. Nếu có bất kỳ thắc mắc nào, bạn hãy liên hệ ngay đến Hotline của AME Group để được hỗ trợ tốt nhất nhé!
 Tiếng Việt
Tiếng Việt